ÁTOMO
Átomo, la unidad más pequeña posible de un elemento químico. En la filosofía de la antigua Grecia, la palabra “átomo” se empleaba para referirse a la parte de materia más pequeño que podía concebirse. Esa “partícula fundamental”, por emplear el término moderno para ese concepto, se consideraba indestructible. De hecho, átomo significa en griego “no divisible”. El conocimiento del tamaño y la naturaleza del átomo avanzó muy lentamente a lo largo de los siglos ya que la gente se limitaba a especular sobre él.
Sin embargo, los avances científicos de este siglo han demostrado que la estructura atómica integra a partículas más pequeñas.
Los científicos y el átomo
Ernest Rutherford, científico nacido en Nueva Zelandia, demostró en 1911 la existencia del núcleo atómico, complementando el conocimiento del electrón, descubierto en 1897 por J.J. Thompson. Desde entonces, múltiples experiencias han demostrado que el núcleo está compuesto por partículas más pequeñas, los protones y neutrones. Y en 1963, Murray Gell-Mann postuló que protones y neutrones están compuestos por partículas aún más pequeñas, a las que llamó "quarks".
La experiencia de Rutherford fue crucial en la determinación de la estructura atómica. Los párrafos que siguen son un extracto de su propia comunicación (1911):
"Es un hecho bien conocido que las partículas alfa y beta sufren desviaciones de sus trayectorias rectilíneas a causa de las interacciones con los átomos de la materia.
Parece indudable que estas partículas de movimiento veloz pasan en su recorrido a través de los átomos, y las desviaciones observadas son debidas al campo eléctrico dentro del sistema atómico.
Las observaciones de Geiger y Mardsen sobre la dispersión de partículas alfa, indican que algunas de estas partículas deben de experimentar en un solo encuentro desviaciones superiores a un ángulo recto.
Un cálculo simple demuestra que el átomo debe de ser asiento de un intenso campo eléctrico para que se produzca una gran desviación en una colisión simple..."
En aquella época Thomson había elaborado un modelo de átomo consistente en un cierto número N de corpúsculos cargados negativamente, acompañados de una cantidad igual de electricidad positiva distribuida uniformemente en toda una esfera. Rutherford pone a prueba este modelo y sugiere el actual modelo de átomo.
"La teoría de Thomson está basada en la hipótesis de que la dispersión debida a un simple choque atómico es pequeña y que la estructura supuesta para el átomo no admite una desviación muy grande de una partícula alfa que incida sobre el mismo, a menos que se suponga que el diámetro de la esfera de electricidad positiva es pequeño en comparación con el diámetro de influencia del átomo.
Puesto que las partículas alfa y beta atraviesan el átomo, un estudio riguroso de la naturaleza de la desviación debe proporcionar cierta luz sobre la constitución del átomo, capaz de producir los efectos observados. En efecto, la dispersión de partículas cargadas de alta velocidad por los átomos de la materia constituyen uno de los métodos más prometedores de ataque del problema.."
En la simulación de la experiencia de Rutherford, consideramos una muestra de un determinado material a elegir entre varios y la situamos en el centro de un conjunto de detectores dispuestos a su alrededor. El blanco es bombardeado por partículas alfa de cierta energía producidas por un material radioactivo. Se observa que muy pocas partículas son desviadas un ángulo apreciable, y se producen muy raramente sucesos en los que la partícula alfa retrocede.
| Modelo atómico de Thomson |
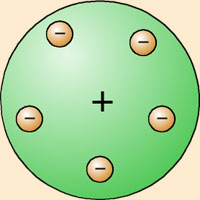 | La identificación por J.J. Thomson de unas partículas subatómicas cargadas negativamente, los electrones, a través del estudio de los rayos catódicos, y su posterior caracterización, le llevaron a proponer un modelo de átomo que explicara dichos resultados experimentales. Se trata del modelo conocido informalmente como elpudín de ciruelas, según el cual los electrones eran como 'ciruelas' negativas incrustadas en un 'pudín' de materia positiva. |
| Modelo atómico de Rutherford |
Rutherford, basándose en los resultados obtenidos en sus experimentos de bombardeo de láminas delgadas de metales, estableció el llamado modelo atómico de Rutherford o modelo atómico nuclear. El átomo está formado por dos partes: núcleo y corteza. El núcleo es la parte central, de tamaño muy pequeño, donde se encuentra toda la carga positiva y, prácticamente, toda la masa del átomo. Esta carga positiva del núcleo, en la experiencia de la lámina de oro, es la responsable de la desviación de las partículas alfa (también con carga positiva). La corteza es casi un espacio vacío, inmenso en relación con las dimensiones del núcleo. Eso explica que la mayor parte de las partículas alfa atraviesan la lámina de oro sin desviarse. Aquí se encuentran los electrones con masa muy pequeña y carga negativa. Como en un diminuto sistema solar, los electrones giran alrededor del núcleo, igual que los planetas alrededor del Sol. Los electrones están ligados al núcleo por la atracción eléctrica entre cargas de signo contrario. |
| Modelo atómico de Bohr |
En 1913 Bohr publicó una explicación teórica para el espectro atómico del hidrógeno. Basándose en las ideas previas de Max Plank, que en 1900 había elaborado una teoría sobre la discontinuidad de la energía (Teoría de los cuantos), Bohr supuso que el átomo solo puede tener ciertos niveles de energía definidos. Bohr establece así, que los electrones solo pueden girar en ciertas órbitas de radios determinados. Estas órbitas sonestacionarias, en ellas el electrón no emite energía: la energía cinética del electrón equilibra exactamente la atracción electrostática entre las cargas opuestas de núcleo y electrón. El electrón solo puede tomar así los valores de energía correspondientes a esas órbitas. Los saltos de los electrones desde niveles de mayor energía a otros de menor energía o viceversa suponen, respectivamente, una emisión o una absorción de energía electromagnética (fotones de luz). |
| Sin embargo el modelo atómico de Bohr también tuvo que ser abandonado al no poder explicar los espectros de átomos más complejos. La idea de que los electrones se mueven alrededor del núcleo en órbitas definidas tuvo que ser desechada. Las nuevas ideas sobre el átomo están basadas en lamecánica cuántica, que el propio Bohr contribuyó a desarrollar. |
Protónes
El protón es una de las partículas subatómicas más importantes. Los protones se combinan con los electrones y (generalmente) con los neutrones para formar átomos.
Los protones son practicamente del mismo tamaño que los neutrones, y ambos son mucho más grandes que los electrones. Un protón tiene una masa aproximadamente 1.836 veces mayor que la masa del electrón, pero las masas de los protones y neutrones se diferencian menos de uno por ciento. Un protón tiene una masa de 1.6726 x 10-24gramos.
Los protones tienen una carga eléctrica positiva, conocida a veces como carga elemental, carga fundamental o carga de +1. Los electrones tienen una carga del mismo valor pero de polaridad opuesta, -1. La carga fundamental tiene un valor de 1.602 x 10-19 coulombios.
El núcleo de un átomo es una combinación de aproximadamente igual cantidad de protones y neutrones, unidos por la muy intensa fuerza nuclear. Nubes de electrones orbitan alrededor del núcleo, atraídas por las cargas positivas de los protones.
Los protones son bariones, una especie de partícula subatómica que también incluye neutrones. Los protones se componen de dos quark arriba y un quark abajo.
El elemento más abundante del universo es el átomo de hidrógeno simple, un electrón que orbita alrededor de un protón. Con frecuencia, los electrones de estos átomos de hidrógeno son desplazados mediante un proceso llamado ionización, lo que deja un solo protón. Tales protones, también llamados iones de hidrógeno (H+), son muy comunes. A causa de sus cargas, estos protones pueden ser acelerados por los campos eléctricos o magnéticos hasta energías muy elevadas y así convertirse en una peligrosa especie de radiación de partículas.descubierto por Ernest Rutherford a principios del siglo XX, el protón es una partícula elemental que constituye parte del núcleo de cualquier átomo. El número de protones en el núcleo atómico, denominado número atómico, es el que determina las propiedades químicas del átomo en cuestión. Los protones poseen carga eléctrica positiva y una masa 1.836 veces mayor de la de los electrones.
El neutrón es una partícula sin carga neta, presente en el núcleo atómico de prácticamente todos los átomos, excepto el propio. Aunque se dice que el neutrón no tiene carga, en realidad está compuesto por tres partículas fundamentales cargadas llamadas quarks, cuyas cargas sumadas son cero. Por tanto, el neutrón es un barión neutro compuesto por dos quarks de tipo abajo, y un quark de tipo arriba.
Fuera del núcleo atómico, los neutrones son inestables, teniendo una vida media de 15 minutos (885.7 ± 0.8 s),;2 cada neutrón se descompone en un electrón, un antineutrino y un protón. Su masa es muy similar a la del protón, aunque ligeramente mayor.
El neutrón es necesario para la estabilidad de casi todos los núcleos atómicos, a excepción del isótopo hidrógeno-1. La interacción nuclear fuerte es responsable de mantenerlos estables en los núcleos atómicos.
constituye parte del núcleo de los átomos. Fueron descubiertos en 1930 por dos físicos alemanes ,Walter Bothe y Herbert Becker. La masa del neutrón es ligeramente superior a la del protón, pero el número de neutrones en el núcleo no determina las propiedades químicas del átomo, aunque sí su estabilidad frente a posibles procesos nucleares (fisión, fusión o emisión de radiactividad). Los neutrones carecen de carga eléctrica, y son inestables cuando se hallan fuera del núcleo, desintegrándose para dar un protón, un electrón y un antineutrino.
Electrónes
Los electrones tienen una masa de 9,11×10-31 kilogramos , unas 1800 veces menor que la de los neutrones y protones. Siendo tan livianos, apenas contribuyen a la masa total de las sustancias. Su movimiento genera la corriente eléctrica, aunque dependiendo del tipo de estructura molecular en la que se encuentren, necesitarán más o menos energía para desplazarse. Estas partículas desempeñan un papel primordial en la química, ya que definen las atracciones entre los átomos.
Desde el punto de vista físico, el electrón tiene una carga eléctrica de igual magnitud, pero de polaridad contraria a la del protón. Dicha magnitud, cuyo valor es de 1,602×10-19 coulombios, es llamada carga elemental o fundamental, y es considera a veces un cuanto de carga eléctrica, asignándosele un valor unitario. Por razones históricas y ventajas en ecuaciones matemáticas, se considera a la carga del protón como positiva, mientras que a la del electrón como negativa. Por esto se dice que los protones y electrones tienen cargas de +1 y -1 respectivamente, aunque esta elección de signo es totalmente arbitraria
partícula elemental que constituye parte de cualquier átomo, descubierta en 1897 por J. J. Thomson. Los electrones de un átomo giran en torno a su núcleo, formando la denominada corteza electrónica. La masa del electrón es 1836 veces menor que la del protón y tiene carga opuesta, es decir, negativa. En condiciones normales un átomo tiene el mismo número de protones que electrones, lo que convierte a los átomos en entidades eléctricamente neutras. Si un átomo capta o pierde electrones, se convierte en un ion.
El electrón comúnmente representado por el símbolo: e−, es una partícula subatómica de tipo termiónico. En un átomo los electrones rodean el núcleo, compuesto únicamente de protones y neutrones.




exelente muy recomendable
ResponderEliminar